アメリカで承認されている医薬品に関するデータベース/データファイル
アメリカの医薬品の承認審査を行うFDA(U.S. Food and Drug Administration)により承認された医薬品の添付文書を調べる方法を概説します。
ちなみに、日本における「添付文書」の内容に近いドキュメントは、アメリカでは「Label」と呼ばれているドキュメントが相当するので、ここではLabelを調べる方法となります。
方法としては色々あるのですが、一番信用できる情報は当然ながらFDAのウェブサイトとなります。
FDAのウェブサイトの中には、医薬品のデータに関するデータベースやデータファイルが用途に合わせて複数存在しいます。
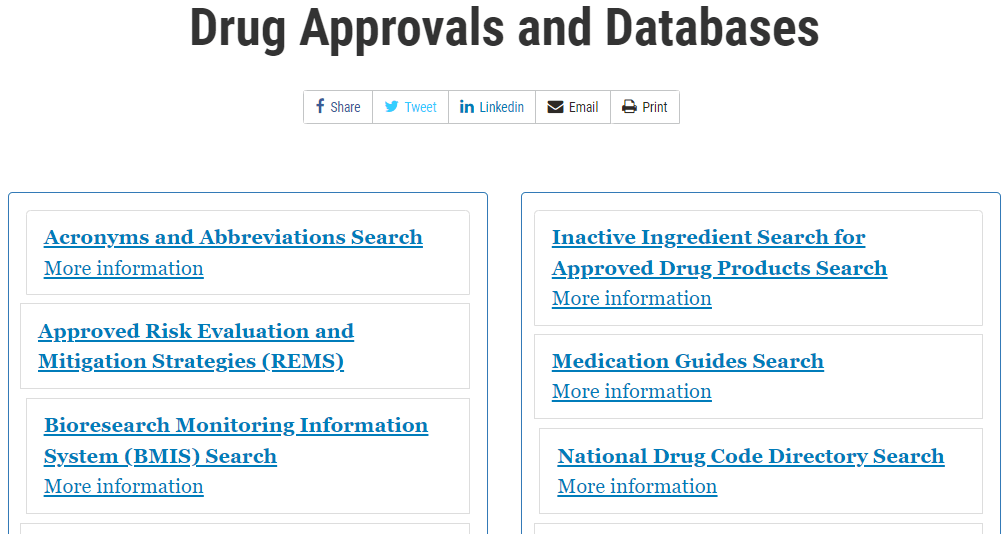
Drug Approvals and Databases
Drugs@FDA Search
20種類を超えるデータベース/データファイルが用意されていますが、この中で添付文書を調べるには「Drugs@FDA Search」を使います。
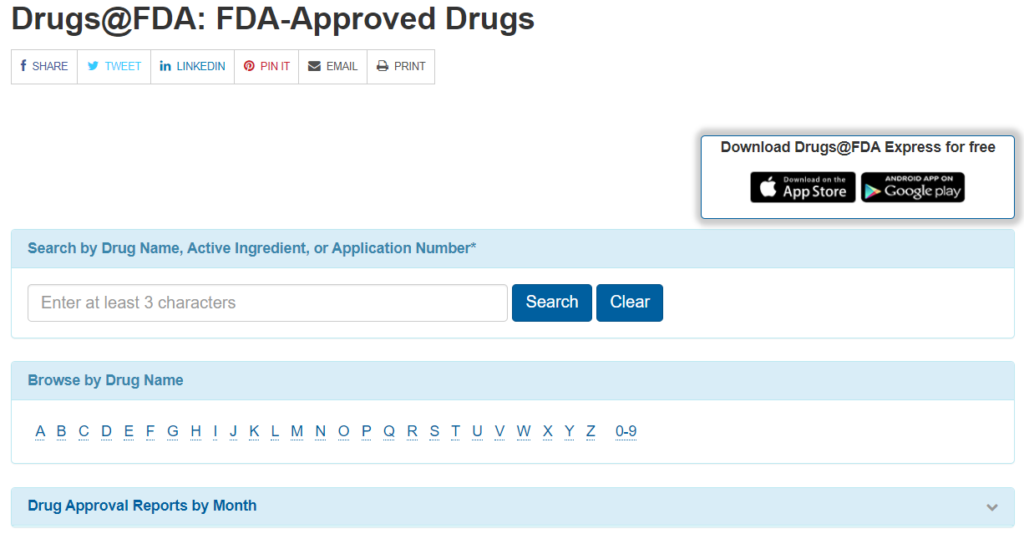
調べ方は3種類あります。
一つ目は薬剤名(一般名、商品名)の部分一致検索、二つ目は商品目 (一般名、商品名) によるリストからの検索、三つ目は承認月毎の品目リストからの検索です。
それぞれが、上の画像の上から「Search by Drug Name, Active Ingredient, or Application Number」、「Browse by Drug Name」、「Drug Approval Reports by Month」に該当します。
ここではオーソドックスに、薬剤名(一般名)からの部分一致による検索を試してみます。
添付文書を検索してみる
ここでは試しに、新型コロナ治療薬で有名になったレムデシビル(Remdesivir)で検索してみます。
一番上の検索フィールドに「Remdesivir」と入力し、「Search」を押下します。
すると、以下のような検索結果が表示されました。
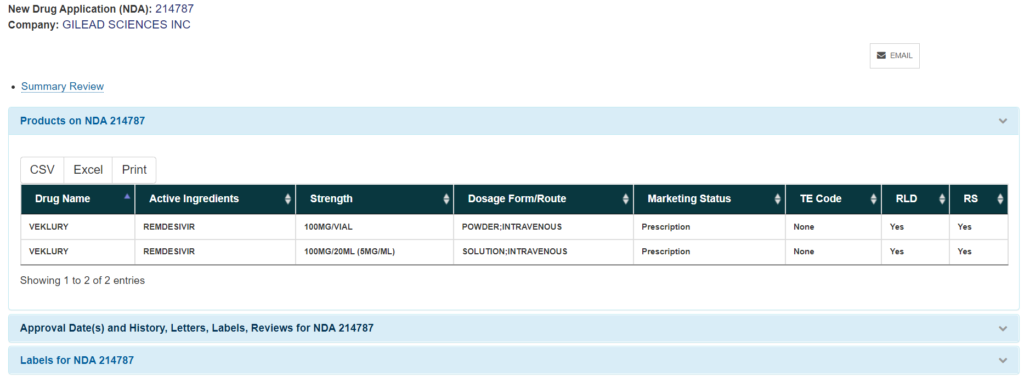
目的としていた添付文書(Label)を閲覧する場合は、3つあるアコーディオンメニューのうち、一番下の「Labels for NDA 214787」を押下し、アコーディオンを開きます。
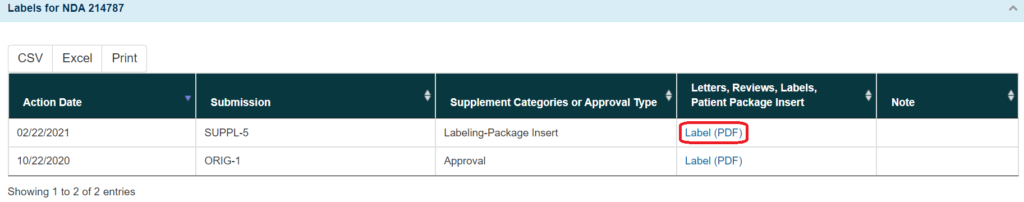
添付文書(Label)は更新されていくものなので、時系列で複数表示されますが、デフォルトでは上にあるファイルが新しいドキュメントとなります。
開いてみると以下のようなファイルが開きます。

最初に「HIGHLIGHTS OF PRESCRIBING INFORMATION」ということで、この医薬品の概要(適応症、投与量・投与方法、禁忌、警告、副作用などの概要)がまとめられています。
Remdesivir(一般名:VEKLURY®)の適応症と処方情報は「INDICATIONS AND USAGE」に
VEKLURY is a SARS-CoV-2 nucleotide analog RNA polymerase inhibitor indicated for adults and pediatric patients (12 years of age and older and weighing at least 40 kg) for the treatment of coronavirus disease 2019 (COVID-19) requiring hospitalization. VEKLURY should only be administered in a hospital or in a healthcare setting capable of providing acute care comparable to inpatient hospital care.
VEKLURYのLabel(2021/2/22 Suppl-5)
と書かれており、ここから「VEKLURYは、入院を要するCOVID-19の治療のために大人と小児(12歳以上かつ体重40kg以上)に対して適応を有するSARS-CoV-2ヌクレオチドアナログRNAポリメラーゼ阻害薬である。VEKLURYは病院または入院治療に匹敵する急性期ケアを提供できる医療環境においてのみ投与すべきである。」ということが分かります。
2ページ目以降は、より詳細な情報が書かれていますので、詳しい情報を知りたい場合には、2ページ目以降を読むことになります。
承認に関するもっと詳しい情報を知りたい場合は?
3つあったアコーディオンメニューの二つ目「Approval Date(s) and History, Letters, Labels, Reviews for NDA 214787」から「Review」を押下します。
品目によっては「Review」がない場合もあります。

すると、「FDA Application Review Files」というボックスから、FDAが承認のための医薬品評価したときのレビューを、医学的視点、化学的視点、薬理学的視点、リスク評価/リスク最小化の視点、統計的視点、細菌学的視点、臨床薬理学的視点など、様々な視点からかなり詳細なレベルで閲覧することができます。
全体的な概要は「Summary Review」から、臨床試験の内容や結果・成績は「Medical Review」や「Statistical Review」から閲覧することで情報を得ることができます(かなり専門的な内容になります)。