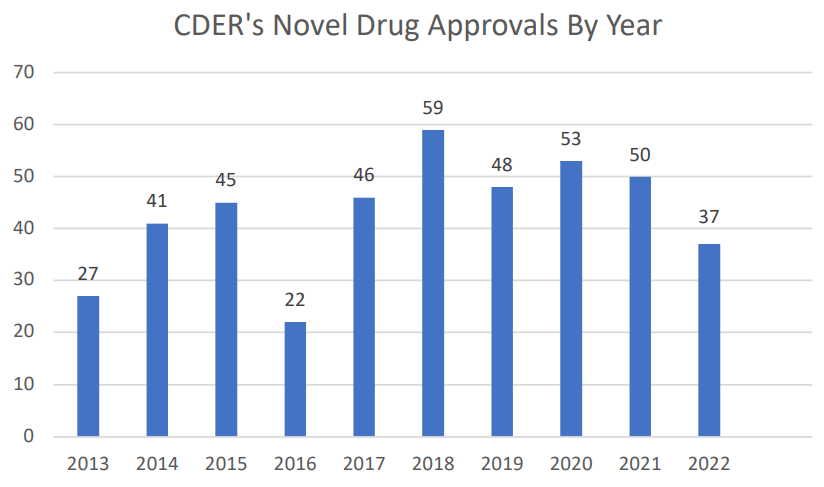
2022年に米国FDAのCDER(The Center for Drug Evaluation and Research)で承認された新薬は37品目となりました。
年間の承認数は、ここ数年では50品目前後で推移していましたので、例年に比べ大幅に減少したように感じるかもしれませんが、過去10年で考えると平均年間承認数は約43品目ですので、それと比べると少し少ないぐらいの印象です。
新型コロナのパンデミックにより世界中で治験の実施が困難になり、治験のスケジュールを延期せざるを得なくなる事態が発生していましたが、その影響が出始めたのかもしれません(そうであれば来年も影響が残っている可能性が高そうです)。
37品目の新薬のうち、25品目(68%)が世界初(=FDAが最初に承認した医薬品)であり、FDAが世界初の承認を与える割合は昨年より少し低下していました(2022年は76%)。
適応症としては、COVID-19、HIV、天然痘、インフルエンザ、ヘリコバクターピロリなどの感染症から、筋萎縮性側索硬化症、糖尿病、貧血、腎障害、炎症性腸疾患、乾癬、炎症性疾患、肺がん、前立腺がんなど多様です。
新規メカニズムの品目は20品目(約54%)でした。
また希少疾病に対する医薬品が全体の約半数(20品目、約54%)を占めており、希少疾病に対する新薬が占める割合も去年とほぼ同じ割合(2021年は52%)でした。
がんや希少疾病の割合が高いとFirst-Trackやブレークスルーなどの承認プロセスの迅速化を目的とした制度の利用が増加する傾向になりますが、実際に2022年において何らかの優先審査制度を利用した品目の割合は65%に達していました。

承認を取得した企業として、ブリストルとジェネンテックが2つ以上の承認を勝ち取っておりますが、全体的にメガファーマの存在感が低下している感じがします。
そんな中で、日本の会社としては参天製薬や大鵬薬品が健闘しました!
日本では、相変わらずの財務省主導による薬価削減策の結果、マーケットとしての日本の魅力が低下し、外資系企業を中心に日本での開発・申請の優先度を下げる会社が増えているようです。
PMDA発足後に理事長に就任された故・近藤先生による力強いリーダーシップにより、PMDAはFDAやEMAと遜色ない能力を持つ医薬品評価機関になり、当時問題となっていたドラッグラグを解消してきましたが、このままではドラッグラグの再発、いや、ドラッグロスが現実になってきそうです。
日本における医薬品のイノベーションに対する適切な評価や開発環境の改善に向けた政策に期待したいところです。
| 商品名 | 成分名 | 申請者 | Orphan | First in Class | First in US |
| Amvuttra | vutrisiran | ALNYLAM PHARMS INC | 〇 | 〇 | |
| Briumvi | ublituximab-xiiy | BIOGEN INC | 〇 | ||
| Camzyos | mavacamten | BRISTOL | 〇 | 〇 | 〇 |
| Cibinqo | abrocitinib | PFIZER | |||
| Daxxify | daxibotulinumtoxinA-lanm | REVANCE THERAPEUTICS, INC. | 〇 | ||
| Elahere | mirvetuximab soravtansine-gynx | IMMUNOGEN INC | 〇 | 〇 | 〇 |
| Elucirem | gadopiclenol | GUERBET | 〇 | ||
| Enjaymo | sutimlimab-jome | BIOVERATIV THERAPEUTICS INC | 〇 | 〇 | 〇 |
| Imjudo | tremelimumab-actl | ASTRAZENECA AB | 〇 | 〇 | |
| Kimmtrak | tebentafusp-tebn | IMMUNOCORE LTD | 〇 | 〇 | 〇 |
| Krazati | adagrasib | MIRATI THERAPS | 〇 | 〇 | |
| Lunsumio | mosunetuzumab-axgb | GENENTECH INC | 〇 | 〇 | |
| Lytgobi | futibatinib | TAIHO ONCOLOGY | 〇 | 〇 | |
| Mounjaro | tirzepatide | ELI LILLY AND CO | 〇 | 〇 | |
| NexoBrid | anacaulase-bcdb | MEDIWOUND, LTD | 〇 | ||
| Omlonti | omidenepag isopropyl | SANTEN | |||
| Opdualag | nivolumab and relatlimab-rmbw | BRISTOL MYERS SQUIBB | 〇 | 〇 | 〇 |
| Pluvicto | lutetium Lu 177 vipivotide tetraxetan | AAA USA NOVARTIS | 〇 | 〇 | |
| Pyrukynd | mitapivat | AGIOS PHARMS INC | 〇 | 〇 | 〇 |
| Quviviq | daridorexant | IDORSIA | 〇 | ||
| Relyvrio | sodium phenylbutyrate and taurursodiol | AMYLYX | 〇 | ||
| Rezlidhia | olutasidenib | RIGEL PHARMS INC | 〇 | 〇 | |
| Rolvedon | eflapegrastim-xnst | SPECTRUM PHARMS | |||
| Sotyktu | deucravacitinib | BRISTOL | 〇 | 〇 | |
| Spevigo | spesolimab-sbzo | BOEHRINGER INGELHEIM PHARMACEUTICALS INC | 〇 | 〇 | 〇 |
| Sunlenca | lenacapavir | GILEAD SCIENCES | 〇 | ||
| Tecvayli | teclistamab-cqyv | JANSSEN BIOTECH | 〇 | 〇 | |
| Terlivaz | terlipressin | MALLINCKRODT IRELAND | 〇 | 〇 | |
| Tzield | teplizumab-mzwv | PROVENTION BIO INC | 〇 | 〇 | |
| Vabysmo | faricimab-svoa | GENENTECH INC | 〇 | ||
| Vivjoa | oteseconazole | MYCOVIA PHARMS | 〇 | ||
| Vonjo | pacritinib | CTI BIOPHARMA CORP | 〇 | 〇 | |
| Voquezna Triple Pak | vonoprazan, amoxicillin, and clarithromycin (co-packaged) | PHATHOM | 〇 | ||
| Vtama | tapinarof | DERMAVANT SCI | 〇 | ||
| Xenoview | hyperpolarized Xe-129 | POLAREAN INC | 〇 | 〇 | |
| Xenpozyme | olipudase alfa-rpcp | GENZYME CORP | 〇 | 〇 | |
| Ztalmy | ganaxolone | MARINUS | 〇 | 〇 | 〇 |
Natureでも2022年におけるFDAにおける医薬品の承認状況を整理した記事がありましたので、ご参考までに以下に載せておきます。